I Généralités.
C’est un système de communication qui permet de mettre l’organisme en relation avec le monde extérieur. Les entrées d’informations se font au niveau de récepteurs sensoriels. Ils ont la capacité de transformer les informations des diverses sources d’énergie en signaux électriques, par un phénomène de transduction. Ces signaux vont gagner les centres nerveux (encéphale, moelle épinière) par les voies afférentes(centripètes) où ils seront traités et codés. Le résultat des traitements est envoyé vers la périphérie sous forme d’ordres moteurs (au sens large) par les voies efférentes. Les organes effecteurs sont : les muscles et glandes endocrines. Le comportement est modifié et/ ou agit en retour sur son environnement.Le système nerveux peut être considéré comme un système de traitement de l’information. Il est capable, grâce à ses constituants (en grande partie les neurones), de créer un signal électrique porteur d’informations et de la transmettre.
II Le neurone.
Les neurones ne sont pas les seules cellules nerveuses. Les cellules gliales, qui s’intercalent entre les neurones, ont un rôle actif dans la régulation des mouvements ioniques. Le neurone est une cellule particulière qui se caractérise par ses prolongements. Certains prolongements sont de forme et de taille variable et constituent les dendrites. Ces dendrites constituent le pôle récepteur de la cellule (en principe).Un prolongement plus important dont le diamètre est relativement constant émerge du soma et constitue l’axone. C’est le pôle émetteur. L’axone se ramifie pour former l’arborisation terminale. Chaque terminaison se finie par un bouton synaptique. L’axone peut présenter des collatérales : ce sont des branches qui se détachent perpendiculairement de l’axone. Ce phénomène permet d’avoir une arborisation très dense. L’axone peut être
très long (plus d’un mètre). Il est entouré d’une gaine de myéline (surtout quand l’axone est long).
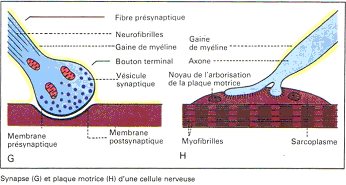
On a différentes classes de neurones :
- Les motoneurones : leur axone est long avec une arborisation dense autour du soma.
- Les neurones pseudo-unipolaires : leur corps cellulaire est rejeté sur le côté avec un prolongement unique.
- Les neurones d’invertébrés : ils ont un soma sans ramification et leur axone présente de nombreuses zones de ramifications. Les zones d’acquisitions et d’émissions sont difficiles à trouver.
- Les cellules rétiniennes.
- Les cellules pyramidales (cortex)…
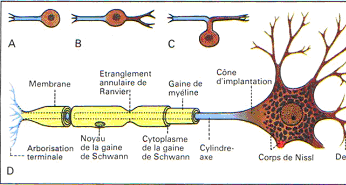
Le neurone présente une régionalisation de ses fonctions qui est due aux propriétés de la membrane plasmique en ses différentes régions (en fonction de la présence de canaux membranaire [protéines] qui ont des propriétés particulières).
III Les propriétés du neurone.
Il y a trois principales propriétés : la capacité d’émettre un potentiel électrique – la conduction : conduire le spike sans diminuer son amplitude – la transmission de l’information vers une autre cellule.Le neurone est capable d’émettre un potentiel électrique qui va correspondre à une variation du potentiel membranaire. Il peut être partiel (variation limitée d’un potentiel local), ou au contraire, maximal et donner un potentiel d’action : l’influx nerveux est le support de l’information. Ces variations de potentiel sont dues à des mouvements ioniques au travers de la membrane plasmique.
A La membrane plasmique.
Elle constitue une barrière entre les milieux intra et extracellulaire par sa nature : double couche (bicouche) lipidique dans laquelle sont incluses des protéines : c’est une mosaïque fluide. Les lipides membranaires sont constitués par des phospholipides, du cholestérol et des glycoprotéines qui présentent une partie hydrophobe et une hydrophile.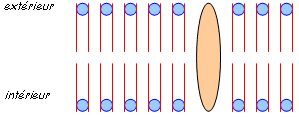
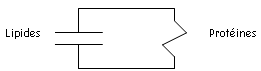
1 Les protéines membranaires.
Le transport passif des ions : selon le gradient électrochimique, on trouve des protéines qui traversent toute la bicouche (canaux axonique et récepteurs aux protéines G). D’autres sont périphériques : du coté cytoplasmique o, a les protéines G, ou, du côté de la fente synaptique (fente cellulaire), des protéines comme l’acétylcholine estérase.Les pompes : transport actif d’ions. Elles sont dans la membrane mais utilisent de l’énergie pour que les ions circulent contre le gradient électrochimique.
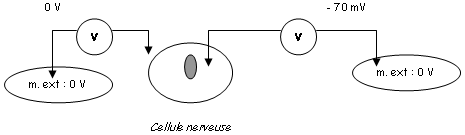
2 Le potentiel de repos du neurone.
[table "6" not found /]
La répartition de ces ions obéie à deux contraintes majeures :
- L’électroneutralité des 2 compartiments (de chaque côté, les milieux doivent être électriquement neutres). A l’extérieur, les charges + sont équilibrées par les ions Cl-. A l’intérieur, les charges + sont équilibrées par des anions qui sont de grosses protéines non diffusibles.
- L’équilibre osmotique : le nombre de particules à l’intérieur et à l’extérieur de la cellule doit être le même quelle que soit leur charge.
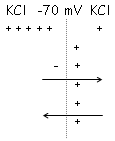
Le potentiel s’équilibre.
Les concentrations ioniques peuvent varier d’un neurone à l’autre. L’électroneutralité n’est pas respectée mais à un niveau microscopique.
La membrane se comporte comme un condensateur limité à la zone où ont lieu les échanges. Le nombre d’ions transférés est très faible. On peut calculer que le transfert de deux ions K+ sur 100 000 est suffisant pour créer la différence de potentiel de –70mV à –80mV.
Les transferts sont donc très réduits. Les concentrations sont faiblement perturbées. Le potentiel peut être calculé à partir de la loi de Nernst :
Eion = [(RT)/(ZF)] x Ln ([K+]ext/[K+]int).
Z est la valence et F, la charge en faraday.
Ei = 58 x log([K+]ext/[K+]int)
Pour chaque ion, le potentiel d’équilibre est : K+ : -84mV ; Na+ : +58mV ; Cl- :-58mV ; Ca2+ : +116mV.
La membrane présente une perméabilité sélective pour chaque ion et le potentiel de repos de la membrane va être défini par l’équation de Goldman.
Vm = (RT/F) x Ln[(Pk x [K]e + Pna x [Na]e + Pcl x [Cl]i)/(Pk x [K]i + Pna x [Na]i + Pcl x [Cl]e)]
Vm = -60mV (c’est une valeur relative)
Au repos, aucun des ions n’est à son potentiel d’équilibre : chaque ion est donc soumis à une force qui correspond à la différence entre le potentiel de repos et le potentiel d’équilibre de l’ion (Vm – Eion). Chaque ion se comporte pour amener la membrane à son potentiel d’équilibre en la traversant. Il en résulte par chacun, un courant ionique proportionnel à cette force qu’est le gradient électrochimique. Le facteur de proportionnalité est « g » : la conductance membranaire pour un ion donné. « g » est la facilité de la membrane à laisser passer l’ion.
I = g x (Vm – Eion)
« g » est différent de la perméabilité membranaire. Quand tous les canaux sont ouverts pour un ion, « g » est indéfini. G = 1/R. « g » se mesure en siemens et il est de l’ordre de 10 à 200 µs (la conductance est toujours positive).
Au repos, cette membrane présente des canaux sélectifs pour chacun des ions.
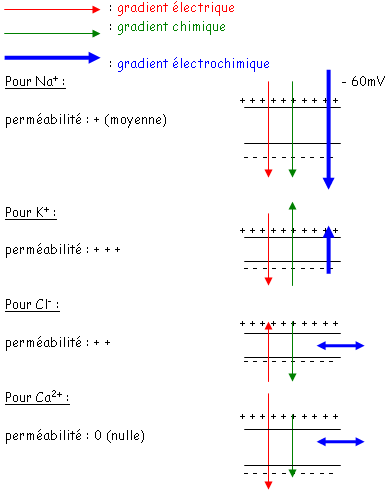
Cependant, les concentrations ioniques de la cellule sont constantes et le potentiel de repos est très stable, ce qui implique que ces mouvements soient en permanence contrebalancés par un phénomène actif qui rejette les ions Na à l’extérieur et fait rentrer les ions K+ à l’intérieur. Ce phénomène actif lutte contre des forces physiques en consommant de l’énergie.
C’est la pompe Na/K. Elle assure ces mouvements ioniques à contre courant en utilisant une grande quantité d’ATP fabriqué par la cellule.
Cette pompe est, elle-même, électrogénique car 2 ions K+ sont récupérés contre 3 Na+ sortis. On a donc un courant positif sortant. C’est l’ensemble de ces phénomènes qui assurent l’équilibre du potentiel de repos (phénomènes actifs + passifs).
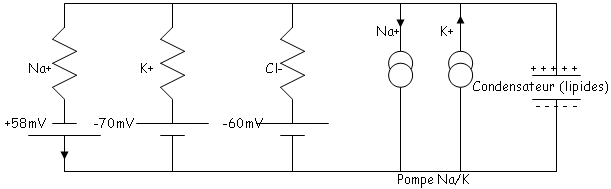
3 Les propriétés électriques passives de la membrane.
Ces diverses propriétés conditionnent la forme et l’amplitude des potentiels locaux.α La résistance membranaire au repos.
Cette résistance est définie par la présence de protéines transmembranaires qui définissent la perméabilité de la membrane au repos de certains ions (donc des canaux passifs). Pour réaliser l’expérience, on injecte dans un neurone, un courant hyper polarisant.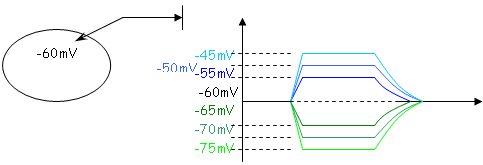
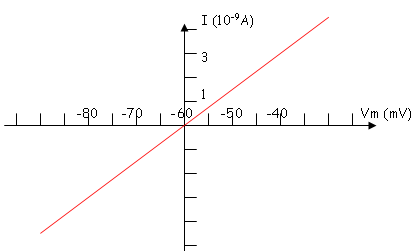
Le facteur de proportionnalité est la résistance membranaire lorsque le neurone est au repos. La résistance de la membrane est de 10MO.
Plus la résistance augmente, plus la variation de potentiel induite par un courant sera importante. Quand le diamètre du neurone diminue, la résistance augmente. Les cellules de petites tailles sont donc plus excitables.
ß La capacité membranaire.
La capacité membranaire est due à la présence des lipides (sont isolants) dans la membrane. Ils vont conduire à l’accumulation de charges opposées de part et d’autre de la membrane. Un courant membranaire va charger le condensateur, mais il a besoin de temps selon le condensateur : on a donc un temps de charge qui influe sur la taille et la forme du potentiel. Le temps de charge augmente avec la surface et l’épaisseur du condensateur : quand le diamètre de la cellule augmente, le temps de charge augmente.On obtient une constante de temps pour chaque cellule (T) : T=R x C. Cette valeur représente le temps au bout duquel la variation de potentiel membranaire a atteint 63% de sa valeur. La constante de temps détermine les capacités d’intégration temporelle d’une cellule.
&gamma: L’influence des résistances transversales et longitudinales.
Cette influence se montre sur la perte d’amplitude du potentiel et sur la vitesse de conduction. La résistance transverse est définie par le nombre de canaux passifs présents dans la membrane. La résistance longitudinale représente la résistance opposée par le milieu cytoplasmique au passage du courant.La résistance transmembranaire est constante sur une portion de membrane donnée alors que la résistance longitudinale, comme tout conducteur, augmente avec la longueur.
Rlong=ρ x (l/s) (s représente la section).
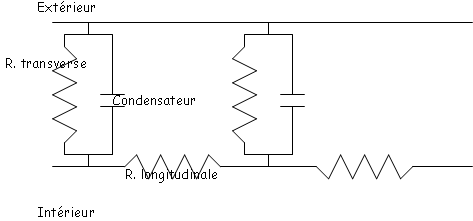
On injecte un courant dépolarisant qui traverse la membrane en plusieurs endroits en empruntant les voies de plus faibles résistances. On observe alors une diminution de l’amplitude du courant quand on s’éloigne du point d’injection du courant. Il s’ensuit alors une baisse progressive du potentiel avec la distance.
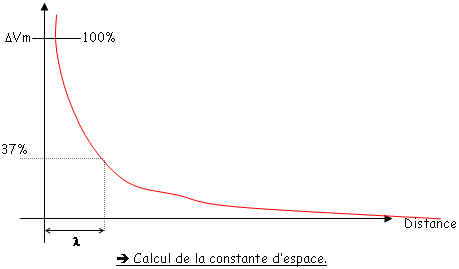
δ Vitesse de conduction.
Comme la résistance longitudinale est inversement proportionnelle à la section de la fibre, plus la fibre est, plus la résistance est faible et donc, la vitesse de conduction s’en trouvera augmentée (c’est vrai pour les dendrites et les axones). L’axone présente un facteur supplémentaire : la myélinisation de la fibre. Celle-ci entraîne une diminution de la capacité membranaire et donc, diminue le temps de charge et augmente la vitesse de conduction.IV Le potentiel d’action.
A Origine/Le voltage clamp.
Dans certaines conditions, la membrane est le siège de variations d’amplitude maximales et constantes : c’est le potentiel d’action. Les potentiels d’action s’observent quand la stimulation du neurone dépasse un certain seuil → stimulations supraliminaires. Dans ces conditions, on a :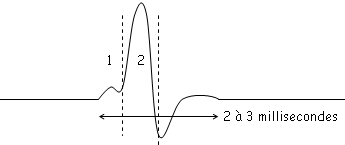
En 2, le potentiel de seuil est atteint → le potentiel d’action va atteindre +45 à +50mV, ce qui correspond à peu près au potentiel d’équilibre du sodium. Le potentiel d’action est du à une augmentation transitoire de la perméabilité membranaire pour le sodium ([Na]ext>[Na]int). La perméabilité membranaire aux ions (surtout pour K+ et Na+) est modifiée pendant le potentiel d’action.
Les expériences de voltage clamp consistent à imposer un saut de potentiel à la membrane. Ce saut est à la base d’un courant qu’on neutralise en injectant dans la cellule un courant de sens opposé. On maintient la membrane au potentiel imposé ; on définit la nature du courant apparu.
Résultats : on enregistre le courant total qui traverse la membrane pour différents sauts de potentiel.
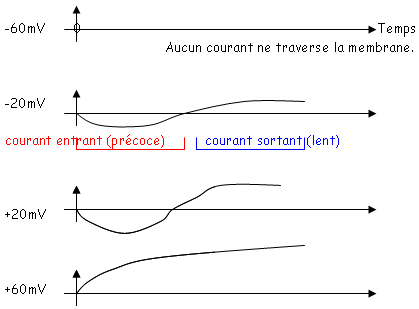
Pour étudier le Na, on utilise du TEA (qui bloque les canaux K+).
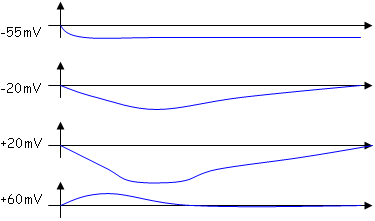
Pour étudier les canaux K+, on utilise la TTX (tétrodotoxine) qui bloque les canaux Na+.
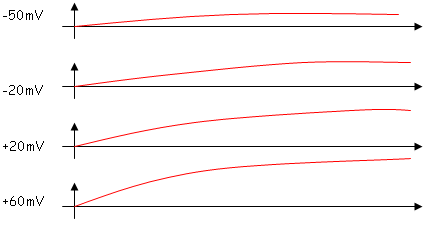
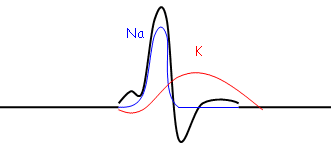
Ce sont ces deux courants qui se développent simultanément pendant le potentiel d’action. Le courant Na assure la phase de dépolarisation membranaire alors que le courant K+ assure la phase de repolarisation membranaire.
Ces courants sont dus à l’augmentation transitoire de la conductance membranaire pour le sodium et le potassium. g=i/(Em-Eion)
B Conduction/Le patch clamp.
On impose un courant sur une portion (on étudie alors un seul canal).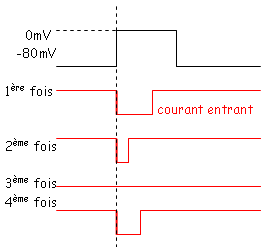
L’ouverture d’un canal dépend de l’intensité de la stimulation (la probabilité d’ouverture augmente avec l’accroissement de l’intensité). Le canal Na présente une porte d’activation
et une d’inactivation.
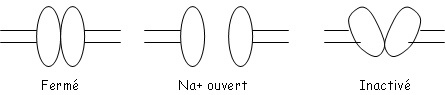
La somme de ces comportements individuels explique l’inactivation spontanée des canaux Na (et du courant Na+).
La rectification retardée.
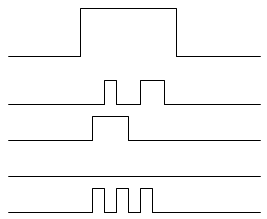
Quand on stimule un neurone avant le potentiel de seuil, on a juste une dépolarisation légère. Si le potentiel de seuil est dépassé, on a un pas. Ce potentiel de seuil est le seuil d’excitation des canaux voltage dépendant (pour les amorcer). Quand les canaux Na s’ouvrent, le sodium rentre et cela continue jusqu’à atteindre l’annulation spontanée et l’augmentation légèrement retardée de la conductance au potassium. La conductance membranaire aux ions dépend de la différence de potentiel membranaire mais aussi du temps.
1 Le potentiel calcique.
Le potentiel d’action n’est pas le seul potentiel présent dans le neurone.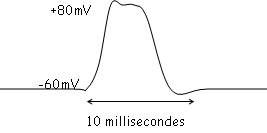
Au cours du potentiel d’action, la concentration calcique intracellulaire augmente beaucoup. Le calcium est souvent à l’origine de déclenchement de voies métaboliques.
La conduction du potentiel d’action se fait donc sans perte d’amplitude et est unidirectionnelle. Si on considère le potentiel d’action à sa naissance, la zone membranaire est dépolarisée alors que la zone adjacente est polarisée : il y a création de courants locaux (courants de fuite). L’intensité de ces courants s’atténue le long de la fibre mais comme les canaux (voltage-dépendants) sont proches, ils sont tout de même activés et, il y a recréation, de proche en proche, du potentiel d’action. On parle de conduction régénérative
sur les axones (alors que sur les dendrites, la conduction est décrémentielle).
Ici, plus l’axone est large, plus la conduction est rapide. Là, la myéline entoure la fibre. Sur les fibres myélinisées, la conduction est saltatoire et la vitesse de conduction s’en trouve augmentée. Les espaces entre la myéline sont appelés « Nœud de Ranvier ». La myéline crée un manchon isolant qui s’oppose au passage du courant tout en diminuant la résistance membranaire et donc, diminue le temps de charge.
L’influx ne peut se reboucler qu’aux nœuds de Ranvier où sont présents de nombreux canaux voltage-dépendants : La vitesse de conduction est fortement augmentée. On trouve en majorité ce type de fibres dans le système nerveux périphérique. La perte de myéline va entraîner de graves pathologies. Par exemple, la démyélinisation du système nerveux central entraîne l’apparition de sclérose en plaque.
Le sens de progression du courant. La progression se fait du soma vers l’arborisation terminale. Le potentiel d’action ne peut pas remonter car les canaux voltage-dépendants situés en amont de la dépolarisation sont dans un état inactif.
V La transmission synaptique.
A Etude des canaux chimio-dépendants.
La jonction neuromusculaire : c’est une connexion entre une fibre motrice et une fibre musculaire : la zone de jonction est appelée « plaque motrice ».Expérience : on provoque une stimulation de l’axone et on enregistre les phénomènes électriques se passant au niveau de la plaque motrice.
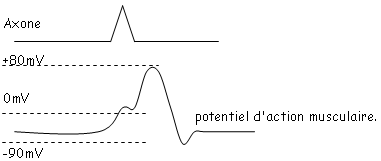
La première dépolarisation correspond à un potentiel post synaptique excitateur (PPSE) : c’est le potentiel de plaque motrice. On montre que ce potentiel local se propage de façon électrique.
B L’origine du potentiel.
En voltage-clamp, on va étudier les courants ioniques mis en œuvre. On prend une plaque motrice à un potentiel imposé. Si on bloque la membrane à –100mV et que l’on provoque une stimulation de l’axone moteur, on enregistre un fort courant rentrant.
Le même résultat est obtenu si l’on injecte de l’acétylcholine dans la fente synaptique au lieu de stimuler l’axone moteur. Les canaux s’ouvrent : ils sont chimio-dépendants. Cette dépolarisation est limitée par la quantité de K+ sortant. Le courant créé par les canaux chimio-dépendants se propage et va stimuler des canaux voltage-dépendants, ce qui explique la seconde phase de la dépolarisation.
Donc : le potentiel d’action arrive au niveau de la terminaison, les canaux voltage-dépendants s’ouvrent, du Ca2+ rentre et il y a libération de neurotransmetteurs. L’acétylcholine se fixe sur les récepteurs nicotiniques (liés à un canal cationique). L’activation de ces récepteurs entraîne un potentiel de plaque motrice qui déclenche un potentiel d’action sur la fibre musculaire par activation de canaux voltage-dépendants.
Ces synapses sont uniquement excitatrices et elles fonctionnent avec un rapport 1/1 (réponse pour tous les potentiels d’action).
Au niveau des synapses de l’encéphale, il existe des synapses excitatrices et des inhibitrices qui peuvent être de types différents en fonction de leur localisation.
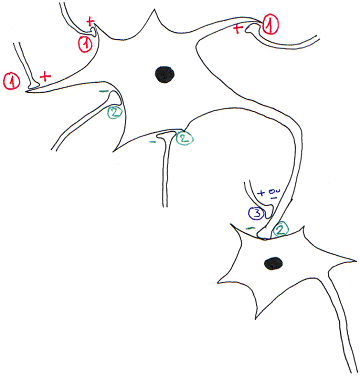
- synapse axo-dendritique.
- synapse axo-somatique.
- synapse axo-axonique (excitatrice ou inhibitrice).
Le neurone va intégrer toutes ces informations (les potentiels d’action infraliminaires qui lui parviennent). Ses caractéristiques (valeur des constantes d’espace et de temps) vont définir les capacités de sommation spatiale et temporelle.
1 sommation spatiale.
Si plusieurs potentiels post-synaptiques excitateurs apparaissent sur des branches dendritiques différentes, ils vont être conduits passivement jusqu’au niveau du cône axonique (baisse d’amplitude avec la distance). Si les pertes sont peu importantes, il va y avoir apparition d’un potentiel d’action. La perte d’amplitude des PPSE est liée à la constante d’espace de chaque dendrite : plus la constante est élevée, plus la perte d’amplitude est réduite. Il en va de même pour les PPSI.2 Sommation temporelle.
La sommation temporelle concerne la sommation en un même point (d’une dendrite) de plusieurs PPS arrivant successivement : plus la constante de temps est élevée, plus la cellule pourra sommer de PPS. La constante de temps définie la capacité de sommation temporelle. T=R x C. T augmente quand le diamètre augmente.C Relation morphologie/caractéristiques.
Au niveau des synapses axo-axoniques, il peut encore y avoir modulation de l’information. La terminaison axonique est dépourvue de canaux voltage-dépendants : le potentiel d’action envahie donc passivement la terminaison de l’axone. Il y aura donc baisse d’amplitude. Cette dernière pourra être modulée par une synapse axo-axonique facilitatrice ou inhibitrice. En conséquence, la modulation du potentiel d’action joue sur la quantité libérée de neurotransmetteurs.VI Les neurotransmetteurs.
Il existe environ une centaine de neurotransmetteurs différents dans le système nerveux central.A Les grandes classes.
- Acides aminés (glutamate, aspartate, gaba, glycine).
- Amines biogènes : adrénaline, noradrénaline, dopamine et sérotonine.
- Acétylcholine.
- Enképhalines (peptides, morphinomimétiques).
- Hormones.
B Principe de fonctionnement.
Certains neurotransmetteurs n’ont qu’un type d’action (ils sont rares) : les acides aminés. Le glutamate et l’aspartate sont excitateurs ; le gaba et la glycine sont présents chez les interneurones inhibiteurs. Tous les neurotransmetteurs ont deux types de récepteurs post synaptiques :- Ionotropiques : le récepteur est directement couplé à un canal ionique. L’action du neurotransmetteur est rapide et correspond toujours à une variation du potentiel de membrane.
- Métabotropiques : le récepteur est couplé à une protéine G membranaire : la fixation du neurotransmetteur entraîne l’activation de messagers secondaires et de voies métaboliques dans la cellule, conduisant, en fonction du type cellulaire, à une excitation ou à une inhibition cellulaire ; ou, à des effets à long terme sur le métabolisme cellulaire.
